根据世界卫生组织统计,癌症已经是世界第二大致死因素。化疗作为治疗癌症的主要手段,但由于缺乏肿瘤选择性,存在较大的毒副作用等问题。前药和药物递送系统是提升抗癌药物的选择性和降低毒副作用的两个有效策略。前药是活性药物的非活性前体,在人体内进行酶代谢从而活化,改善母体药物的药代动力学特征。药物递送系统可以将化疗药物靶向递送到肿瘤部位,提高治疗效果和控制药物释放。分子印迹聚合物(MIP)已经被广泛应用于药物递送,但MIP和前药的联合使用,此前未见文献报道。
近日,我院刘震课题组报道了一种基于分子印迹技术的纳米智能前药递送策略,论文发表于Angew. Chem. Int. Ed.(2020, DOI:10.1002/anie.202012956),为我校化学学科百年华诞献礼。该策略以分子印迹纳米颗粒为载体,具有特异性靶向肿瘤细胞,长时间肿瘤部位保留,以及肿瘤微环境触发释放药物的特点。不同于传统的前药需要依赖肝脏的生物转化,该分子印迹前药递送体系是肿瘤依赖性的,而非肝脏依赖性的,避免了肝脏部位酶的影响。该工作为发展智能前药递送纳米载体开辟了新的路径。
对于MIP的合成,作者利用课题组自主研发的先进印迹技术—硼亲和定向可控表面印迹法(Angew. Chem. Int. Ed., 2015, 54, 10211-10215;Nat. Protocol., 2017, 12, 964–987),将目标前药5-脱氧-5-氟胞苷(DFCR)(卡培他滨的一级代谢产物)和癌症靶标唾液酸(SA)共印迹到纳米粒子上,形成双模板分子印迹聚合物(dt-MIP);当携带了DFCR的dt-MIP到达肿瘤部位时,该纳米载体能通过与SA结合而靶向识别癌细胞,同时长时间保留在肿瘤部位;在该条件下,DFCR缓慢从该载体中释放出来,被癌细胞摄取,经过两部酶转化(胞苷脱氨酶,胸苷磷酸化酶),生成活性分子5-氟尿嘧啶(FU),诱导癌细胞死亡(原理见图1)。
分子印迹
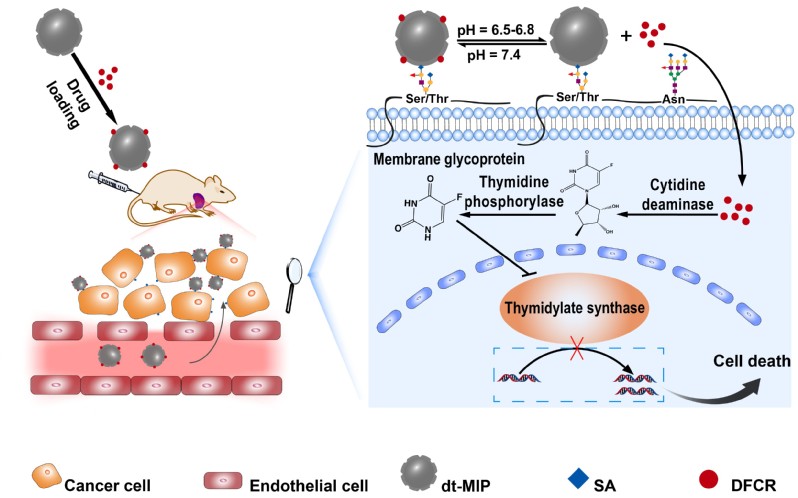
图1. 双模板分子印迹聚合物载药递送原理图 作者通过共聚焦荧光和流式细胞术,证明了dt-MIP对于癌细胞的靶向能力(图2)。紧接着,作者证实了载药dt-MIP可以被pH = 6.8的酸性微环境触发,可控释放药物(pH = 7.4时不释放)。同时,载药dt-MIP与HepG-2共孵育48h后,细胞抑制率为58%,证实了载药dt-MIP的细胞毒性(图3)。同时,作者考察了不同材料在荷瘤裸鼠体内的分布,相比于非靶向的纳米粒子,dt-MIP可以在肿瘤部位保留更长的时间(10天)(图4)。最后,作者考察了载药dt-MIP的抑瘤效果,相比起空白对照组(PBS)和裸药对照组(DFCR),载药dt-MIP具有最佳的肿瘤抑制效果(图5)。
分子印迹
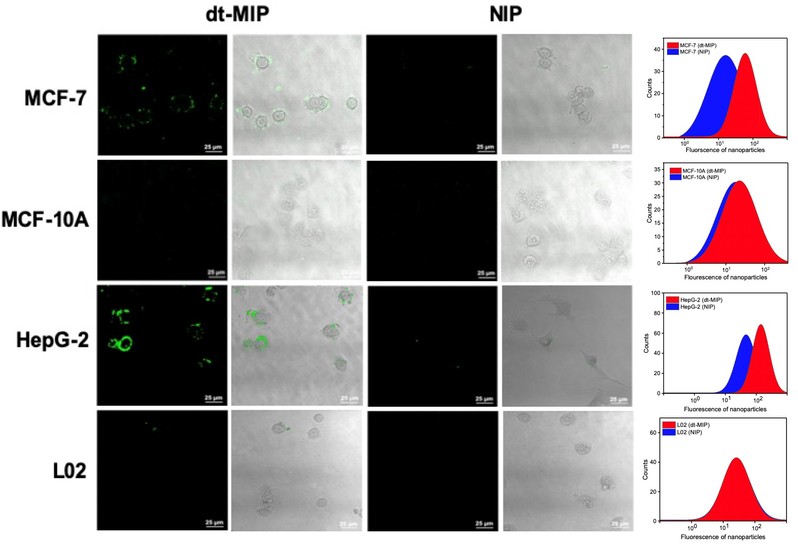
图2. dt-MIP对于过表达SA的癌细胞系和不表达SA的正常细胞系特异性靶向实验结果
分子印迹
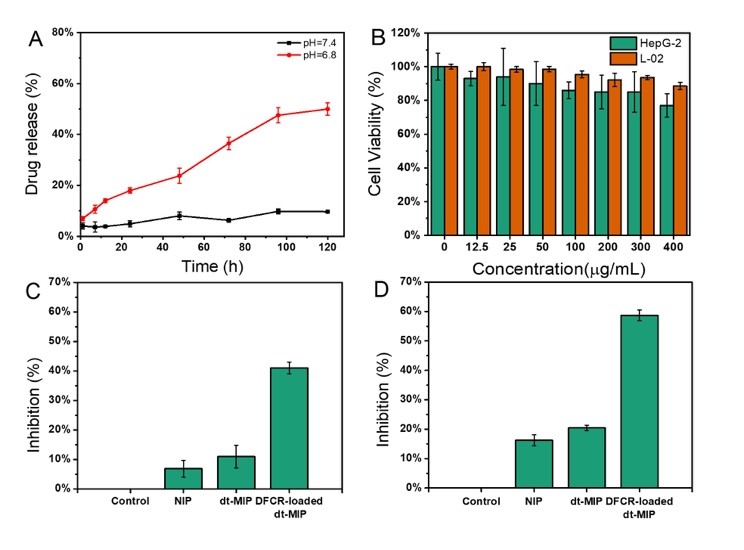
图3. A) 不同pH 条件下的药物释放曲线;B) 细胞抑制率实验结果
分子印迹
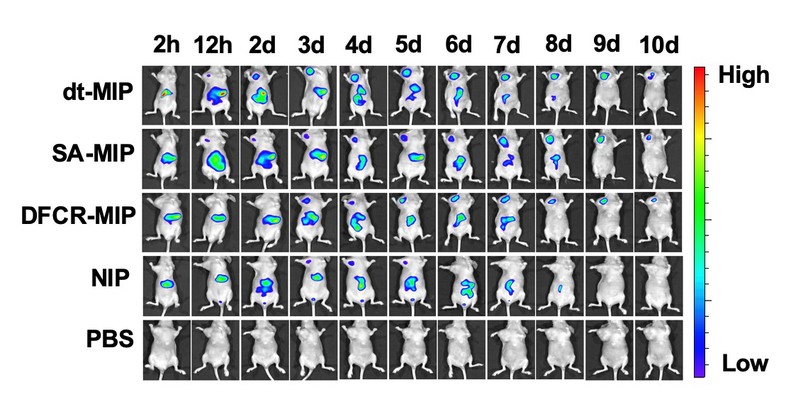
图4. 注射不同材料的荷瘤裸鼠的体内荧光分布
分子印迹
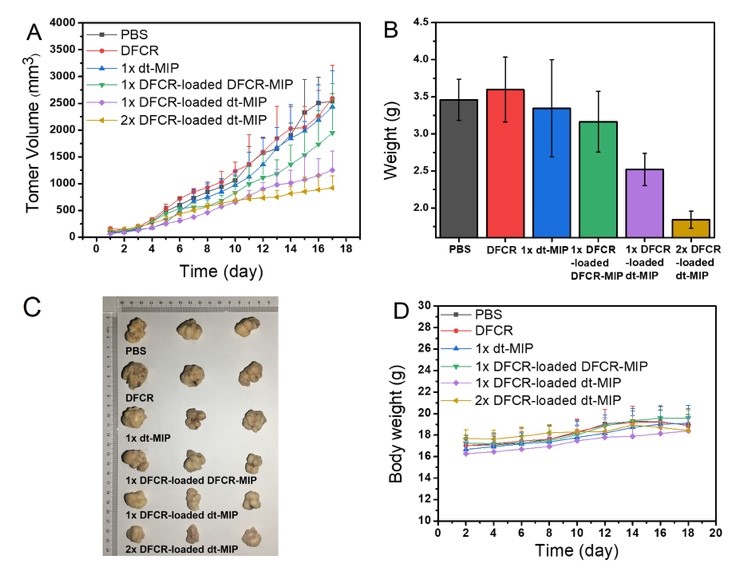
图5. 荷瘤裸鼠抑瘤实验结果
该论文的通讯作者为我院刘震教授,我院博士研究生顾自宽和已毕业硕士生董月茹为共同作者,我院许舒欣博士和加拿大渥太华大学医学院Lisheng Wang教授为共同作者。该工作得到国家自然科学基金重点项目(21834003)、国家重点研发计划(2018YFC0910301)和南京大学卓越计划(ZYJH004)等的经费支持。
刘震教授课题组在分子印迹技术用于抗肿瘤方面已连续取得重要进展(Chem. Comm. 2017, 53, 6716-6719; Angew. Chem. Int. Ed. 2019, 58, 10621-10625)。最近,课题组综述了近年来MIP在抗肿瘤方面的最新进展(Angew. Chem. Int. Ed. 2020,DOI: 10.1002/anie.202005309)。
全文链接:https://onlinelibrary.wiley.com/doi/10.1002/ange.202012956
文章来源:南京大学
刘震,1970年出生,博士,教授,博士生导师,国家杰出青年基金获得者。1992年于贵州大学获理学学士学位,1995年于南京大学获理学硕士学位,1998年7月于中国科学院大连化学物理研究所获理学博士学位。2000年1月至2002年1月,日本兵库大学(University of Hyogo)日本学术振兴会(JSPS)特别研究员;2002年8月至2005年11月,加拿大滑铁卢大学(University of Waterloo)博士后;2005年12月起任南京大学化学化工学院教授;2006年3月起为博士生导师;2008年入选教育部“新世纪优秀人才”;2009年入选南京大学“优秀中青年学科带头人”;2011年-2014年任加拿大滑铁卢大学兼职教授;2011年入选江苏省“333高层次人才”(第三层次);2014年获国家杰出青年科学基金。兼任国际分子印迹学会理事会理事、中国化学会质谱专业委员会委员、中国生物化学与分子生物学会蛋白质组学专业委员会委员和《色谱》杂志编委等职。获中国分析测试协会科学技术奖一等奖(2011)。主要从事分子识别、生物分离和疾病标志物分析研究,主要代表性成果有基于硼亲和作用的仿生分子识别、亲和分离介质及生命分析新方法。出版专著1本,专章5章,发表SCI论文100余篇(IF>3,80余篇;IF>5, 40余篇),引用3000余次。申请发明专利17项,其中8项已获授权。
| 